Mga pamamaraan para sa pagtukoy ng aldehydes at ketones. Ketones
Aldehydes at ketones.
Ang mga aldehydes at ketone ay may magkatulad na istrukturang kemikal. Samakatuwid, ang kuwento tungkol sa kanila ay pinagsama sa isang kabanata.
Ang istraktura ng parehong mga compound ay naglalaman ng isang divalent carbonyl group:
Ang pagkakaiba sa pagitan ng aldehydes at ketones ay ang mga sumusunod. Sa aldehydes, ang carbonyl group ay nakagapos sa isang hydrogen atom at isang hydrocarbon radical, habang sa ketones ito ay nakagapos sa dalawang hydrocarbon radical.

Mga kemikal na katangian ng aldehydes at ketones.
Ang pagkakaroon ng isang carbonyl group sa parehong aldehydes at ketones ay tumutukoy sa isang tiyak na pagkakatulad sa kanilang mga katangian. Gayunpaman, mayroon ding mga pagkakaiba.
Ang pagkakaiba na ito ay ipinaliwanag sa pamamagitan ng pagkakaroon sa molekula ng aldehyde ng isang hydrogen atom na nakagapos sa pangkat ng carbonyl. (Walang ganoong atom sa molekula ng ketone)..

Ang carbonyl group at ang hydrogen atom na nauugnay dito ay pinaghihiwalay sa isang hiwalay na functional group. Pinangalanan ang grupong ito
aldehyde functional group

Dahil sa pagkakaroon ng hydrogen sa molekula ng aldehyde, ang huli ay madaling na-oxidized (nagdagdag ng oxygen) at na-convert sa mga carboxylic acid.
Halimbawa, ang oksihenasyon ng acetaldehyde ay gumagawa ng acetic acid:
Dahil sa kanilang madaling oksihenasyon, ang mga aldehydes ay mga energetic na nagpapababa ng ahente. Ginagawa nitong makabuluhang naiiba ang mga ito sa mga ketone, na mas mahirap i-oxidize. Paghahanda ng aldehydes at ketones.
Ang mga aldehydes at ketone ay maaaring ihanda sa pamamagitan ng oksihenasyon ng mga kaukulang alkohol
pagkakaroon ng parehong carbon skeleton at hydroxyl sa parehong carbon atom, na bumubuo ng carbonyl group sa nagreresultang aldehyde o ketone.
Kung ang isang pangunahing alkohol ay ginagamit bilang ang na-oxidized na alkohol, ang oksihenasyon ay magreresulta sa isang aldehyde.

Formic aldehyde (formaldehyde).
ay ang pinakasimpleng aldehyde na may formula:
Ang formaldehyde ay nakuha mula sa methyl alcohol, ang pinakasimpleng alkohol.
Sa formaldehyde, ang radical ay isang hydrogen atom.
Mga Katangian:
ay isang gas na may masangsang na hindi kanais-nais na amoy, lubos na natutunaw sa tubig. Mayroon itong antiseptic at tanning properties. mula sa methyl alcohol sa pamamagitan ng catalytic oxidation na may atmospheric oxygen o sa pamamagitan ng dehydrogenation (pag-aalis ng hydrogen).

Application:
Ang isang may tubig na solusyon ng formaldehyde (karaniwan ay 40%) ay tinatawag formaldehyde. Ang Formalin ay malawakang ginagamit para sa pagdidisimpekta at pag-iingat ng anatomical specimens. Ang mga makabuluhang halaga ng formaldehyde ay ginagamit upang makagawa ng phenol-formaldehyde resins.
Ito ay isa sa pinakamahalagang aldehydes. Ito ay tumutugma ethyl alcohol at maaaring makuha sa pamamagitan ng oksihenasyon nito.

Acetaldehyde malawak na matatagpuan sa kalikasan at ginawa sa maraming dami sa industriya. Ito ay naroroon sa kape, hinog na prutas, tinapay, at na-synthesize ng mga halaman bilang resulta ng kanilang metabolismo.
Ang formaldehyde ay nakuha mula sa methyl alcohol, ang pinakasimpleng alkohol.
Acetaldehyde– bahagyang kumukulong walang kulay na likido (punto ng kumukulo 21 degrees C). Ito ay may katangiang amoy ng bulok na mansanas at lubos na natutunaw sa tubig.
Mga Katangian:
Sa industriya acetaldehyde ito ay lumabas:
- oksihenasyon ng ethylene,
- pagdaragdag ng tubig sa acetylene,
- oksihenasyon o dehydrogenation ng ethyl alcohol.
Application:
Mag-apply acetaldehyde para sa produksyon ng acetic acid, butadiene, ilang mga organikong sangkap, aldehyde polymers.
Dimethyl ketone (acetone).
Dimethyl ketone (acetone) ay ang pinakasimpleng ketone. Sa molekula nito, ang papel ng mga hydrocarbon radical ay nilalaro ng methyl CH 3(nalalabi sa methane).

Ang formaldehyde ay nakuha mula sa methyl alcohol, ang pinakasimpleng alkohol.
Acetone– walang kulay na likido na may katangiang amoy.
Boiling point 56,2 digri SA.
Acetone hinahalo sa tubig sa lahat ng sukat.
Ito ay isa sa mga metabolite na ginawa ng katawan ng tao.
Mga Katangian:
- Acetone maaaring makuha sa pamamagitan ng oksihenasyon ng propene,
- Mga pamamaraan na ginamit upang makuha acetone mula sa isopropyl alcohol at acetylene,
- Pangunahing bahagi acetone nakuha bilang isang co-product sa produksyon ng phenol mula sa benzene gamit ang cumene method.
Application:
Acetone- Napaka magandang solvent maraming mga organikong sangkap. Malawakang ginagamit sa industriya ng pintura at barnis, sa paggawa ng ilang uri ng artipisyal na hibla, hindi nababasag na organikong salamin, pelikula, at walang usok na pulbos. Acetone ginagamit din bilang panimulang materyal para sa synthesis ng isang bilang ng mga organikong compound.
1. Oksihenasyon ng mga alkohol. Ang mga pangunahing alkohol sa panahon ng oksihenasyon ay bumubuo ng mga aldehydes, na pagkatapos ay madaling ma-oxidize sa mga carboxylic acid:
Ang oksihenasyon ng pangalawang alkohol ay gumagawa ng mga ketone:
2. Hydration ng alkynes (Kucherov reaction). Ang pagdaragdag ng tubig sa acetylene sa pagkakaroon ng mercury (II) salts ay humahantong sa pagbuo ng acetaldehyde:
Ang mga ketone ay nakukuha sa pamamagitan ng hydration ng iba pang acetylene homologues:
3. Oxidation ng mga alkenes (catalysts - Pd at Cu chlorides):
4. Paraan ng Cumene para sa paggawa ng acetone at phenol (Kruzhalov, Sergeev, Nemtsov):
5. Reaksyon ng oxosynthesis:
6. Pagbawas ng carboxylic acid chlorides:
7. Ang mga carbonyl compound ay mga intermediate na produkto ng oksihenasyon ng hydrocarbons sa mga acid.
Mga kemikal na katangian ng aldehydes at ketones. Tinutukoy ng elektronikong istraktura ng pangkat ng carbonyl ang reaktibiti ng aldehydes at ketones. Ang carbon atom ng carbonyl group ay nasa estado ng sp 2 hybridization. Ang anggulo ng bono sa pagitan ng mga δ-bond ay 120 0. Ang unpaired p-electron ng carbon ay nagsasapawan sa p-electron ng oxygen at bumubuo ng π-bond, na matatagpuan patayo sa eroplano ng aldehyde molecule. Ang densidad ng elektron ng π bond ay inililipat patungo sa oxygen. Batay dito, ang mga tipikal na reaksyon ng aldehydes at ketones ay:
─ nucleophilic substitution reactions (Ad N);
─ mga reaksyon ng oksihenasyon;
─ mga reaksyong kinasasangkutan ng mga atomo ng hydrogen sa α-posisyon sa pangkat ng carbonyl.
Mga reaksyon sa pagdaragdag ng nucleophilic. Ang mga reaksyon ng pagdaragdag ng nucleophilic ay nagpapatuloy sa yugto ng pagbuo ng isang intermediate complex, na nailalarawan sa pamamagitan ng pagbabago sa uri ng hybridization ng panimulang aldehyde. Ang molekula ay gumagamit ng uri ng hybridization na magiging sa mga huling produkto ng reaksyon. Ang mekanismo ng reaksyon ay:
1. Pakikipag-ugnayan sa hydrocyanic acid:
Ang mga ketone ay mas mahirap na pumasok sa mga reaksyon ng Ad N kaysa sa aldehydes. Ito ay dahil sa steric hindrance ng mga alkyl radical ng ketones sa panahon ng pagbuo ng intermediate na istraktura.
2. Pagdaragdag ng sodium hydrosulfite:
Ang mga methyl ketones lamang ang tumutugon sa sodium hydrosulfite.
Ang mga reaksyon ng mga carbonyl compound na may sodium hydrosulfite ay ginagamit upang linisin ang mga produkto mula sa mga carbonyl compound.
3. Pakikipag-ugnayan sa ammonia:
Ang pakikipag-ugnayan ng mga ketone sa ammonia ay nangyayari nang iba:
4. Pakikipag-ugnayan sa hydroxylamine. Kapag ang mga carbonyl compound ay tumutugon sa hydroxylamine, ang mga oxime ay nabuo:
Ang reaksyong ito ay ginagamit para sa quantitative determination ng carbonyl compounds sa reaction mixtures at iba't ibang produkto. Sa kasong ito, ginagamit ang hydroxylamine hydrochloride (NH 2 -OH HCl).
5. Pakikipag-ugnayan ng aldehydes sa hydrazine:
Ang mga ketone ay nakikipag-ugnayan sa katulad na paraan.
6. Pakikipag-ugnayan sa phenylhydrosine:
7. Mga reaksyon ng hydrogenation. Kapag ang aldehydes ay nabawasan, ang mga pangunahing alkohol ay nabuo. Kapag ang mga ketone ay nabawasan, ang mga pangalawang alkohol ay nabuo. Kapag ang mga ketone ay nabawasan ng hydrogen sa oras ng paglabas, ang pagbuo ng mga pinacone ay posible.
8. Pakikipag-ugnayan ng aldehydes sa mga alkohol:
Mga reaksyon ng oksihenasyon. Ang oksihenasyon ng mga carbonyl compound ay nangyayari sa ilalim ng banayad na mga kondisyon. Ang mga aldehydes ay na-oxidized sa mga carboxylic acid. Ang mga ketone ay na-oxidized sa isang halo ng mga acid na may pagkaputol ng hydrocarbon chain:
Mga reaksyon ng salamin na pilak.
 Aldehydes– mga organikong sangkap na ang mga molekula ay naglalaman ng pangkat ng carbonyl C=O, konektado sa isang hydrogen atom at isang hydrocarbon radical.
Aldehydes– mga organikong sangkap na ang mga molekula ay naglalaman ng pangkat ng carbonyl C=O, konektado sa isang hydrogen atom at isang hydrocarbon radical.
Ang pangkalahatang formula ng aldehydes ay:

Sa pinakasimpleng aldehyde, formaldehyde, ang papel ng isang hydrocarbon radical ay ginagampanan ng isa pang hydrogen atom:

Ang isang carbonyl group na nakagapos sa isang hydrogen atom ay madalas na tinatawag aldehydic:
Ketones– mga organikong sangkap sa mga molekula kung saan ang pangkat ng carbonyl ay nauugnay sa dalawang radikal na hydrocarbon. Malinaw, ang pangkalahatang formula para sa mga ketone ay:

Ang carbonyl group ng ketones ay tinatawag pangkat ng keto.
Sa pinakasimpleng ketone, acetone, ang carbonyl group ay naka-link sa dalawang methyl radical:

Nomenclature at isomerism ng aldehydes at ketones
Depende sa istraktura ng hydrocarbon radical na konektado sa pangkat ng aldehyde, ang saturated, unsaturated, aromatic, heterocyclic at iba pang mga aldehydes ay nakikilala:

Alinsunod sa IUPAC nomenclature, ang mga pangalan ng saturated aldehydes ay nabuo mula sa pangalan ng isang alkane na may parehong bilang ng mga carbon atom sa molekula gamit ang suffix. -al. Halimbawa:

Ang pagbilang ng mga carbon atom ng pangunahing kadena ay nagsisimula sa carbon atom ng aldehyde group. Samakatuwid, ang pangkat ng aldehyde ay palaging matatagpuan sa unang carbon atom, at hindi na kailangang ipahiwatig ang posisyon nito.
Kasama ng systematic nomenclature, ginagamit din ang mga trivial na pangalan ng malawakang ginagamit na aldehydes. Ang mga pangalang ito ay karaniwang hinango sa mga pangalan ng mga carboxylic acid na nauugnay sa aldehydes.
Upang pangalanan ang mga ketone ayon sa sistematikong nomenclature, ang pangkat ng keto ay itinalaga ng suffix -Siya at isang numero na nagsasaad ng bilang ng carbon atom ng pangkat ng carbonyl (dapat magsimula sa dulo ng chain na pinakamalapit sa pangkat ng keto). Halimbawa:
Ang mga aldehydes ay nailalarawan sa pamamagitan lamang ng isang uri ng structural isomerism - isomerism ng carbon skeleton, na posible sa butanal, at para sa ketones din ang isomerism ng posisyon ng carbonyl group. Bilang karagdagan, ang mga ito ay nailalarawan sa pamamagitan ng interclass isomerism (propanal at propanone).

Mga pisikal na katangian ng aldehydes
Sa isang aldehyde o ketone molecule, dahil sa mas malaking electronegativity ng oxygen atom kumpara sa carbon atom, ang bond C=O mataas na polarized dahil sa isang pagbabago sa density ng elektron π - mga bono sa oxygen:

Ang mga aldehydes at ketones ay mga polar substance na may labis na densidad ng elektron sa oxygen atom. Ang mas mababang mga miyembro ng serye ng mga aldehydes at ketones (formaldehyde, acetaldehyde, acetone) ay walang limitasyong natutunaw sa tubig. Ang kanilang mga boiling point ay mas mababa kaysa sa mga katumbas na alkohol. Ito ay dahil sa ang katunayan na sa mga molekula ng aldehydes at ketones, hindi katulad ng mga alkohol, walang mga mobile na atomo ng hydrogen at hindi sila bumubuo ng mga iniuugnay dahil sa mga bono ng hydrogen. Ang mas mababang aldehydes ay may masangsang na amoy; Ang mga aldehyde na naglalaman ng apat hanggang anim na carbon atom sa kadena ay may hindi kanais-nais na amoy; ang mas mataas na aldehydes at ketones ay may mga bulaklak na amoy at ginagamit sa pabango .

Mga kemikal na katangian ng aldehydes at ketones
Ang pagkakaroon ng isang pangkat ng aldehyde sa isang molekula ay tumutukoy sa mga katangian ng aldehydes.
1. Reaksyon ng pagbabawas.
Ang pagdaragdag ng hydrogen sa mga molekula ng aldehyde ay nangyayari sa pamamagitan ng dobleng bono sa pangkat ng carbonyl. Ang produkto ng hydrogenation ng aldehydes ay mga pangunahing alkohol, at ang mga ketone ay pangalawang alkohol. Kaya, kapag ang hydrogenating acetaldehyde sa isang nickel catalyst, ang ethyl alcohol ay nabuo, at kapag ang hydrogenating acetone, 2-propanol ay nabuo.

Hydrogenation ng aldehydes- isang reduction reaction kung saan bumababa ang oxidation state ng carbon atom na kasama sa carbonyl group.
2. Mga reaksyon ng oksihenasyon. Ang mga aldehydes ay hindi lamang mababawasan, kundi pati na rin mag-oxidize. Kapag na-oxidize, ang mga aldehydes ay bumubuo ng mga carboxylic acid.
Oksihenasyon sa pamamagitan ng oxygen ng hangin. Halimbawa, ang propionic acid ay nabuo mula sa propionic aldehyde (propanal):

Oxidation na may mahinang oxidizing agent(ammonia solution ng silver oxide).

Kung ang ibabaw ng sisidlan kung saan isinasagawa ang reaksyon ay dati nang degreased, kung gayon ang pilak na nabuo sa panahon ng reaksyon ay sumasakop dito ng isang manipis, kahit na pelikula. Ito ay gumagawa ng isang kahanga-hangang pilak na salamin. Samakatuwid, ang reaksyong ito ay tinatawag na "salamin na pilak" na reaksyon. Ito ay malawakang ginagamit para sa paggawa ng mga salamin, mga dekorasyong pilak at mga dekorasyon ng Christmas tree.
3. Reaksyon ng polimerisasyon:
n CH 2 =O → (-CH 2 -O-) n paraform n=8-12
Paghahanda ng aldehydes at ketones

Paglalapat ng aldehydes at ketones
Formaldehyde(methanal, formic aldehyde) H 2 C=O:
a) para sa paggawa ng phenol-formaldehyde resins;
b) pagkuha ng urea-formaldehyde (urea) resins;
c) polyoxymethylene polymers;
d) synthesis ng mga gamot (urotropine);
e) disimpektante;
e) isang preservative para sa biological na paghahanda (dahil sa kakayahang mag-coagulate ng mga protina).
Acetaldehyde(ethanol, acetaldehyde) CH 3 CH=O:
a) paggawa ng acetic acid;
b) organikong synthesis.
Acetone CH 3 -CO-CH 3:
a) solvent para sa mga barnis, pintura, cellulose acetates;
b) hilaw na materyales para sa synthesis ng iba't ibang mga organikong sangkap.
Mga nilalaman ng artikulo
ALDEHYDES AT KETONES– mga organikong compound na naglalaman ng isang >C=O fragment (carbon na naka-link ng double bond sa oxygen, ito ay tinatawag na carbonyl). Sa aldehydes, ang carbonyl carbon ay konektado sa H atom at ang organikong pangkat R (pangkalahatang formula RHC=O), at sa mga ketones - sa dalawang organikong grupo (pangkalahatang formula R 2 C=O).
Nomenclature ng aldehydes at ketones. Ang pangkat na –(H)C=O ay tinatawag na aldehyde; ito ay mayroon lamang isang libreng valence upang magbigkis sa mga organikong grupo, ito ay nagpapahintulot na ito ay matatagpuan lamang sa dulo ng hydrocarbon chain (ngunit hindi sa gitna). Kapag kino-compile ang pangalan ng isang aldehyde, ang pangalan ng kaukulang hydrocarbon ay ipinahiwatig, kung saan idinagdag ang suffix na "al", halimbawa, methanal H 2 C=O, ethanal H 3 CC(H)=O, propanal H 3 CCH 2 C(H)=O. Sa mas kumplikadong mga kaso, ang carbon chain ng R group ay binibilang, simula sa carbonyl carbon, pagkatapos ay gumagamit ng mga numerical na indeks upang ipahiwatig ang posisyon ng mga functional na grupo at iba't ibang mga substituent.
kanin. 1. NOMENCLATURE NG ALDEHYDES. Ang mga pagpapalit at functional na grupo, pati na rin ang kanilang kaukulang mga digital na indeks, ay naka-highlight sa iba't ibang kulay.
Para sa ilang aldehydes, ang mga trivial (pinasimple) na pangalan na nabuo sa kasaysayan ay kadalasang ginagamit, halimbawa, formaldehyde H 2 C=O, acetaldehyde H 3 CC(H)=O, crotonaldehyde CH 3 CH=CHC(H)=O.
Hindi tulad ng pangkat ng aldehyde, ang pangkat ng ketone >C=O ay maaari ding matatagpuan sa gitna ng kadena ng hydrocarbon, samakatuwid, sa mga simpleng kaso, ipahiwatig ang mga pangalan ng mga organikong grupo (binabanggit ang mga ito sa pataas na pagkakasunud-sunod) at idagdag ang salitang "ketone" : dimethyl ketone CH 3 –CO–CH 3 , methyl ethyl ketone CH 3 CH 2 –CO–CH 3 . Sa mas kumplikadong mga kaso, ang posisyon ng pangkat ng ketone sa hydrocarbon chain ay ipinahiwatig ng isang digital index, pagdaragdag ng suffix " Siya" Ang pag-numero ng hydrocarbon chain ay nagsisimula mula sa dulo na mas malapit sa ketone group (Larawan 2).

kanin. 2. NOMENCLATURE NG KETONES. Ang mga pagpapalit at functional na grupo at ang kanilang mga kaukulang digital na indeks ay naka-highlight sa iba't ibang kulay.
Para sa pinakasimpleng ketone CH 3 –CO–CH 3 tinatanggap ang maliit na pangalan - acetone.
Mga kemikal na katangian ng aldehydes at ketones
ay tinutukoy ng mga katangian ng pangkat ng carbonyl >C=O, na may polarity - ang densidad ng elektron sa pagitan ng mga atomo ng C at O ay hindi pantay na ipinamamahagi, inilipat sa mas electronegative O atom Bilang resulta, ang pangkat ng carbonyl ay nakakakuha ng mas mataas na reaktibiti. na ipinapakita sa iba't ibang mga reaksyon sa karagdagan sa dobleng bono. Sa lahat ng mga kaso, ang mga ketone ay hindi gaanong reaktibo kaysa sa mga aldehydes, sa partikular, dahil sa steric na hadlang na nilikha ng dalawang organic na grupo ng R, ang formaldehyde H 2 C=O ay pinakamadaling lumahok sa mga reaksyon.
1. Pagdaragdag sa pamamagitan ng double bond C=O.
Kapag nakikipag-ugnayan sa mga alkohol, ang aldehydes ay bumubuo ng hemiacetals - mga compound na naglalaman ng parehong alkoxy at isang hydroxy group sa isang carbon atom: >C(OH)OR. Ang mga hemiacetals ay maaaring higit pang mag-react sa isa pang molekula ng alkohol, na bumubuo ng buong acetals - mga compound kung saan ang isang carbon atom ay sabay na naglalaman ng dalawang pangkat ng RO: >C(OR) 2. Ang reaksyon ay na-catalyzed ng mga acid at base (Larawan 3A). Sa kaso ng mga ketone, ang pagdaragdag ng mga alkohol sa double bond sa C=O ay mahirap.
Sa katulad na paraan, ang mga aldehydes at ketone ay tumutugon sa hydrocyanic acid HCN, na bumubuo ng mga hydroxynitriles - mga compound na naglalaman ng OH at CN group sa isang carbon atom: >C(OH)Cє N (Fig. 3B). Ang reaksyon ay kapansin-pansin dahil pinapayagan nito ang carbon chain na tumaas (lumalabas ang isang bagong C-C bond).
Sa parehong paraan (pagbubukas ng C=O double bond), ammonia at amines ay tumutugon sa mga aldehydes at ketones, ang mga produkto ng karagdagan ay hindi matatag at nag-condense sa paglabas ng tubig at pagbuo ng isang C=N double bond. Sa kaso ng ammonia, ang mga imine ay nakuha (Larawan 3C), at mula sa mga amin na tinatawag na mga base ng Schiff ay nabuo - mga compound na naglalaman ng fragment > C = NR (Larawan 3D). Ang produkto ng pakikipag-ugnayan ng formaldehyde na may ammonia ay medyo naiiba - ito ay ang resulta ng cyclization ng tatlong intermediate molecules, na nagreresulta sa framework compound hexamethylenetetramine, na ginagamit sa gamot bilang ang gamot na urotropine (Fig. 3D).

2. Mga reaksyon ng condensation. Para sa mga aldehydes at ketones, ang condensation ay posible sa pagitan ng dalawang molekula ng parehong tambalan. Sa gayong paghalay ng mga aldehydes, nagbubukas ang dobleng bono ng isa sa mga molekula, na bumubuo ng isang tambalang naglalaman ng parehong aldehyde at isang pangkat ng OH, na tinatawag na aldol (aldehyde alcohol). Ang condensation na nangyayari ay tinatawag na aldol, at ang reaksyong ito ay na-catalyzed ng mga base (Larawan 4A). Ang resultang aldol ay maaaring higit pang mag-condense upang bumuo ng C=C double bond at maglalabas ng condensation water. Ang resulta ay isang unsaturated aldehyde (Fig. 4A, crotonaldehyde). Ang condensation na ito ay tinatawag na crotonic condensation pagkatapos ng pangalan ng unang tambalan sa serye ng unsaturated aldehydes. Ang mga ketones ay may kakayahang lumahok din sa aldol condensation (Fig. 4B), ngunit ang pangalawang yugto, croton condensation, ay mahirap para sa kanila. Ang mga molekula ng iba't ibang aldehydes, pati na rin ang isang aldehyde at isang ketone, ay maaaring magkasamang lumahok sa aldol condensation sa lahat ng kaso, ang carbon chain ay humahaba. Ang crotonaldehyde na nakuha sa huling yugto (Fig. 4A), na nagtataglay ng lahat ng mga katangian ng aldehydes, ay maaaring higit pang lumahok sa aldol at croton condensation kapag nakikipag-ugnayan sa susunod na bahagi ng acetaldehyde kung saan ito nakuha (Fig. 4B). Sa ganitong paraan, posibleng pahabain ang kadena ng hydrocarbon, na nakakakuha ng mga compound kung saan ang mga single at double bond ay kahalili: –CH=CH–CH=CH–.

Ang condensation ng aldehydes at ketones na may phenols ay nagsasangkot ng pag-alis ng carbonyl O atom (sa anyo ng tubig), at ang methylene group na CH2 o isang substituted methylene group (CHR o CR2) ay ipinasok sa pagitan ng dalawang phenol molecule. Ang reaksyong ito ay pinakamalawak na ginagamit upang makabuo ng phenol-formaldehyde resins (Larawan 5).

kanin. 5. CONDENSATION NG PHENOL NA MAY FORMALDEHYDE
3. Ang polimerisasyon ng mga carbonyl compound ay nangyayari sa pagbubukas ng C=O double bond at pangunahing katangian ng aldehydes. Kapag ang mga may tubig na solusyon ng formaldehyde ay sumingaw sa vacuum, isang halo ng mga cyclic compound (pangunahin ang trioxymethylene) at mga linear na produkto na may maliit na haba ng chain n = 8-12 (paraforms) ay nabuo. Sa pamamagitan ng polymerizing ng cyclic na produkto, ang polyformaldehyde ay nakuha (Larawan 6), isang polimer na may mataas na lakas at mahusay na mga katangian ng insulating elektrikal, na ginagamit bilang isang istrukturang materyal sa paggawa ng mekanikal at instrumento.

kanin. 6. MGA PRODUKTO NG FORMALDEHYDE POLYMERIZATION
4. Pagbawas at oksihenasyon. Ang mga aldehydes at ketone ay parang mga intermediate compound sa pagitan ng mga alcohol at carboxylic acid: ang pagbabawas ay humahantong sa mga alkohol, at ang oksihenasyon ay humahantong sa mga carboxylic acid. Sa ilalim ng pagkilos ng H2 (sa pagkakaroon ng isang Pt o Ni catalyst) o iba pang pagbabawas ng mga reagents, halimbawa, LiAlH4, ang mga aldehydes ay nabawasan, na bumubuo ng mga pangunahing alkohol, at mga ketone - pangalawang alkohol (Larawan 7, mga scheme A at B).
Ang oksihenasyon ng mga aldehydes sa mga carboxylic acid ay nangyayari nang madali sa pagkakaroon ng O 2 o sa ilalim ng pagkilos ng mga mahinang ahente ng pag-oxidizing, tulad ng isang ammonia solution ng silver hydroxide (Fig. 7B). Ang kamangha-manghang reaksyon na ito ay sinamahan ng pagbuo ng isang pilak na salamin sa panloob na ibabaw ng aparato ng reaksyon (karaniwan ay isang ordinaryong tubo ng pagsubok na ginagamit para sa husay na pagtuklas ng pangkat ng aldehyde); Hindi tulad ng mga aldehydes, ang mga ketone ay mas lumalaban sa oksihenasyon kapag pinainit sa pagkakaroon ng mga malakas na ahente ng pag-oxidizing, halimbawa, KMnO 4, ang mga mixtures ng mga carboxylic acid ay nabuo na may pinaikling (kumpara sa orihinal na ketone) na hydrocarbon chain.

kanin. 7. PAGBAWAS AT OXIDATION NG ALDEHYDES AT KETONES
Ang karagdagang kumpirmasyon na ang mga aldehydes ay sumasakop sa isang intermediate na posisyon sa pagitan ng mga alkohol at mga acid ay ang reaksyon na nagreresulta sa isang alkohol at isang carboxylic acid mula sa dalawang molekula ng aldehyde (Larawan 8A), i.e. ang isang molekula ng aldehyde ay na-oxidized at ang isa ay nabawasan. Sa ilang mga kaso, ang dalawang resultang compound—isang alkohol at isang carboxylic acid—ay higit na tumutugon sa isa't isa, na bumubuo ng isang ester (Larawan 8B).

kanin. 8 . SABAY NA OXIDATION AT PAGBAWAS NG ALDEHYDES
Halimbawa, ang oksihenasyon ng acetaldehyde ay gumagawa ng acetic acid:
Ang pinaka-unibersal na paraan ay ang oksihenasyon ng mga alkohol, kung saan ang mga aldehydes ay nabuo mula sa mga pangunahing alkohol, at ang mga ketone mula sa pangalawang alkohol (Larawan 9A at B). Ito ang mga kabaligtaran na reaksyon sa mga nasa Fig. 7A at B. Ang reaksyon ay mababaligtad kung ang aktibong reagent (oxidizing agent sa halip na ang reducing agent) at ang catalyst ay binago ang isang tansong catalyst ay epektibo sa oksihenasyon ng mga alkohol.
Sa industriya, ang acetaldehyde ay nakuha sa pamamagitan ng oksihenasyon ng ethylene (Larawan 9B), ang isang alkohol ay nabuo kung saan ang pangkat ng OH ay "katabi" sa dobleng bono (vinyl alcohol ay hindi matatag at kaagad); isomerize sa carbonyl compounds. Ang isa pang paraan ay ang catalytic hydration ng acetylene (Fig. 9D), ang intermediate compound ay vinyl alcohol. Kung kukuha ka ng methyl acetylene sa halip na acetylene, makakakuha ka ng acetone (Larawan 9E). Ang pang-industriya na paraan para sa paggawa ng acetone ay ang oksihenasyon ng cumene. Ang mga aromatic ketone, tulad ng acetophenone, ay ginawa ng catalytic na pagdaragdag ng isang acetyl group sa isang aromatic ring (Larawan 9E).

Application ng aldehydes at ketones.
Ang formaldehyde H 2 C=O (ang may tubig na solusyon nito ay tinatawag na formalin) ay ginagamit bilang isang leather tanning agent at isang preservative para sa biological na paghahanda.
Ang Acetone (CH 3) 2 C=O ay isang malawakang ginagamit na extractant at solvent para sa mga barnis at enamel.
Aromatic ketone benzophenone (C 6 H 5) 2 C=O na may amoy ng geranium, na ginagamit sa mga komposisyon ng pabango at para sa pampalasa na sabon.
Ang ilan sa mga aldehydes ay unang natagpuan sa mga mahahalagang langis ng halaman at kalaunan ay artipisyal na na-synthesize.
Aliphatic aldehyde CH 3 (CH 2) 7 C (H) = O (ang walang kuwentang pangalan ay pelargonaldehyde) ay matatagpuan sa mahahalagang langis ng mga halamang sitrus, may amoy ng orange, at ginagamit bilang pampalasa ng pagkain.
Ang aromatic aldehyde vanillin (Larawan 10) ay matatagpuan sa mga bunga ng tropikal na halaman ng banilya;

kanin. 10. VANILLIN
Ang Benzaldehyde C 6 H 5 C (H) = O na may amoy ng mapait na almendras ay matatagpuan sa almond oil at sa eucalyptus essential oil. Ang sintetikong benzaldehyde ay ginagamit sa mga esensya ng lasa ng pagkain at komposisyon ng pabango.
Ang Benzophenone (C 6 H 5) 2 C=O at ang mga derivatives nito ay may kakayahang sumipsip ng mga sinag ng UV, na tumutukoy sa kanilang paggamit sa mga suntan cream at lotion bilang karagdagan, ang ilang benzophenone derivatives ay may aktibidad na antimicrobial at ginagamit bilang mga preservative. Ang benzophenone ay may kaaya-ayang amoy ng geranium, at samakatuwid ito ay ginagamit sa mga komposisyon ng pabango at para sa pampalasa na sabon.
Ang kakayahan ng mga aldehydes at ketones na lumahok sa iba't ibang mga pagbabagong-anyo ay tumutukoy sa kanilang pangunahing paggamit bilang panimulang mga compound para sa synthesis ng iba't ibang mga organikong sangkap: alkohol, carboxylic acid at kanilang mga anhydride, gamot (urotropine), mga produktong polimer (phenol-formaldehyde resins, polyformaldehyde), sa paggawa ng lahat ng uri ng mabangong sangkap (batay sa benzaldehyde) at mga tina.
Mikhail Levitsky
Ang unang pangkat ng mga katangian ay mga reaksyon sa karagdagan. Sa pangkat ng carbonyl, mayroong isang dobleng bono sa pagitan ng carbon at oxygen, na, tulad ng naaalala mo, ay binubuo ng isang sigma bond at isang pi bond. Bilang karagdagan sa mga reaksyon, ang pi bond ay nasira at dalawang sigma bond ay nabuo, ang isa ay may carbon at ang isa ay may oxygen. Ang isang bahagyang positibong singil ay puro sa carbon, at isang bahagyang negatibong singil sa oxygen. Samakatuwid, ang isang negatibong sisingilin na reagent particle, isang anion, ay nakakabit sa carbon, at isang positibong sisingilin na bahagi ng molekula ay nakakabit sa oxygen.
Una hydrogenation ng ari-arian, pagdaragdag ng hydrogen.
Ang reaksyon ay nangyayari kapag pinainit. Ang kilala nang hydrogenation catalyst nickel ay ginagamit. Ang mga pangunahing alkohol ay nakukuha mula sa aldehydes, at pangalawang alkohol mula sa mga ketone.
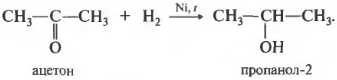
Sa pangalawang alkohol, ang pangkat ng hydroxo ay nakatali sa pangalawang carbon atom.
Pangalawa hydration ng ari-arian, pagdaragdag ng tubig. Ang reaksyong ito ay posible lamang para sa formaldehyde at acetaldehyde. Ang mga ketone ay hindi tumutugon sa tubig.
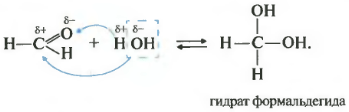
Ang lahat ng mga reaksyon sa karagdagan ay nagpapatuloy sa paraang ang plus ay napupunta sa minus, at minus sa plus.
Tulad ng naaalala mo mula sa video tungkol sa mga alkohol, ang pagkakaroon ng dalawang grupo ng hydroxo sa isang atom ay isang halos imposibleng sitwasyon ang mga naturang sangkap ay lubhang hindi matatag. Kaya ang dalawang partikular na kaso na ito - hydrate ng formaldehyde at acetaldehyde - ay posible, bagama't umiiral lamang ang mga ito sa solusyon.
Hindi kailangang malaman ang mga reaksyon mismo. Malamang, ang tanong sa pagsusulit ay maaaring mukhang isang pahayag ng katotohanan, halimbawa, ang mga sangkap ay tumutugon sa tubig at nakalista. Kabilang sa mga ito, maaaring kabilang sa listahan ang methanal o ethanal.
Pangatlo pagdaragdag ng pag-aari ng hydrocyanic acid.

Muli, ang plus ay napupunta sa minus, at minus sa plus. Ang mga nagresultang sangkap ay tinatawag na hydroxynitriles. Muli, ang reaksyon mismo ay hindi pangkaraniwan, ngunit ito ay isang pag-aari na nagkakahalaga ng pag-alam.
Pang-apat pagdaragdag ng ari-arian ng mga alkohol.
Dito muli, hindi mo kailangang malaman ang equation ng reaksyon sa pamamagitan ng puso, kailangan mo lamang na maunawaan na posible ang gayong pakikipag-ugnayan.

Gaya ng dati sa mga reaksyon ng karagdagan sa isang carbonyl group, plus sa minus, at minus sa plus.
Panglima reaksyon ng ari-arian na may sodium hydrosulfite.

At muli, ang reaksyon ay medyo kumplikado, hindi malamang na matutunan mo ito, ngunit ito ay isa sa mga husay na reaksyon sa aldehydes, dahil ang nagresultang sodium salt ay namuo. Iyon ay, sa katunayan, dapat mong malaman na ang aldehydes ay tumutugon sa sodium hydrosulfite, ito ay magiging sapat.
Nagtatapos ito sa unang pangkat ng mga reaksyon. Ang pangalawang pangkat ay polymerization at polycondensation reactions.
2. Polymerization at polycondensation ng aldehydes
Pamilyar ka sa polymerization: polyethylene, butadiene at isoprene rubbers, polyvinyl chloride - ito ay mga produkto ng pagsasama-sama ng maraming molekula (monomer) sa isang malaki, solong polymer chain. Ibig sabihin, isang produkto ang nakuha. Sa panahon ng polycondensation, ang parehong bagay ay nangyayari, ngunit bilang karagdagan sa polimer, ang mga produktong mababa ang molekular na timbang ay nakuha din, halimbawa, tubig. Ibig sabihin, dalawang produkto ang nakuha.
Kaya, pang-anim polymerization ng ari-arian. Ang mga ketone ay hindi pumapasok sa mga reaksyong ito; tanging ang polimerisasyon ng formaldehyde ang mahalaga sa industriya.
Ang pi bond break at dalawang sigma bond ay nabuo kasama ng mga kalapit na monomer. Ang resulta ay polyformaldehyde, na tinatawag ding paraform. Malamang, ang tanong sa pagsusulit ay maaaring ganito: ang mga sangkap ay pumapasok sa mga reaksyon ng polimerisasyon. At mayroong isang listahan ng mga sangkap na maaaring kabilang ang formaldehyde.
Ang ikapitong ari-arian ay polycondensation. Muli: sa panahon ng polycondensation, bilang karagdagan sa polimer, ang isang mababang molekular na timbang na tambalan ay nakuha din, halimbawa, tubig. Ang formaldehyde ay tumutugon sa phenol sa ganitong paraan. Para sa kalinawan, isinusulat muna namin ang equation na may dalawang molekulang phenol.

Bilang isang resulta, ang naturang dimer ay nabuo at isang molekula ng tubig ay nahati. Ngayon isulat natin ang equation ng reaksyon sa pangkalahatang anyo.

Ang produktong polycondensation ay phenol-formaldehyde resin. Mayroon itong malawak na hanay ng mga aplikasyon, mula sa mga pandikit at barnis hanggang sa mga plastik at mga bahagi ng chipboard.
Ngayon ang ikatlong pangkat ng mga katangian - mga reaksyon ng oksihenasyon.
3. Oxidation ng aldehydes at ketones
ikawalo ang reaksyon sa pangkalahatang listahan ay isang husay na reaksyon sa pangkat ng aldehyde - oksihenasyon na may solusyon sa ammonia ng silver oxide. Ang reaksyon ng "salamin na pilak". Sasabihin ko kaagad na ang mga ketone ay hindi pumapasok sa reaksyong ito, mga aldehydes lamang.

Ang pangkat ng aldehyde ay na-oxidized sa isang carboxyl, acidic na grupo, ngunit sa pagkakaroon ng ammonia, na isang base, isang reaksyon ng neutralisasyon ay agad na nangyayari at ang asin na ammonium acetate ay nakuha. Ang pilak ay namuo, pinahiran ang loob ng test tube at lumilikha ng parang salamin na ibabaw. Ang reaksyong ito ay nangyayari sa Unified State Exam sa lahat ng oras.
Sa pamamagitan ng paraan, ang parehong reaksyon ay husay para sa iba pang mga sangkap na may isang pangkat ng aldehyde, halimbawa, formic acid at mga asing-gamot nito, pati na rin ang glucose.
ikasiyam ang reaksyon ay husay din sa aldehyde group oxidation na may bagong precipitated copper hydroxide two. Dito ko rin mapapansin na ang mga ketone ay hindi pumapasok sa reaksyong ito.

Biswal, ang pagbuo ng isang dilaw na precipitate ay unang makikita, na pagkatapos ay nagiging pula. Sa ilang mga aklat-aralin mayroong impormasyon na ang unang tanso hydroxide ay nabuo, na may dilaw na kulay, na pagkatapos ay nasira sa pulang tansong oksido at tubig. Kaya hindi ito totoo - ayon sa pinakabagong data, sa panahon ng proseso ng pag-ulan, nagbabago ang laki ng mga particle ng tanso oksido, na sa huli ay umaabot sa mga sukat na may kulay na pula. Ang aldehyde ay na-oxidized sa kaukulang carboxylic acid. Ang reaksyon ay madalas na nangyayari sa Unified State Examination.
Ikasampung reaksyon: oksihenasyon ng aldehydes na may acidified na solusyon ng potassium permanganate kapag pinainit.
Ang solusyon ay nagiging kupas. Ang pangkat ng aldehyde ay na-oxidized sa isang pangkat ng carboxyl, iyon ay, ang aldehyde ay na-oxidized sa kaukulang acid. Para sa mga ketones, ang reaksyong ito ay walang praktikal na kahulugan, dahil ang molekula ay nawasak at ang resulta ay isang halo ng mga produkto.
Mahalagang tandaan na ang formic aldehyde, formaldehyde, ay na-oxidized sa carbon dioxide, dahil ang kaukulang formic acid nito ay hindi lumalaban sa malakas na oxidizing agent.
Bilang resulta, ang carbon ay napupunta mula sa oxidation state 0 hanggang oxidation state +4. Hayaan akong ipaalala sa iyo na ang methanol, bilang panuntunan, sa ilalim ng gayong mga kondisyon ay na-oxidized sa maximum na CO 2, na nilaktawan ang yugto ng parehong aldehyde at acid. Ang tampok na ito ay dapat tandaan.
Pang-labing-isa reaksyon pagkasunog, kumpletong oksihenasyon. Ang parehong mga aldehydes at ketone ay nasusunog sa carbon dioxide at tubig.
Isulat natin ang equation ng reaksyon sa pangkalahatang anyo.
Ayon sa batas ng konserbasyon ng masa, dapat mayroong kasing dami ng mga atomo sa kaliwa gaya ng mga atomo sa kanan. Dahil sa mga reaksiyong kemikal, ang mga atomo ay hindi nawawala, ngunit ang pagkakasunud-sunod ng mga bono sa pagitan nila ay nagbabago lamang. Kaya magkakaroon ng kasing dami ng mga molekula ng carbon dioxide gaya ng mayroong mga carbon atom sa isang molekula ng isang carbonyl compound, dahil ang molekula ay naglalaman ng isang carbon atom. Iyon ay, n CO 2 molecules. Magkakaroon ng dalawang beses na mas kaunting mga molekula ng tubig kaysa sa mga atomo ng hydrogen, iyon ay, 2n/2, na nangangahulugang n lamang.
Mayroong parehong bilang ng mga atomo ng oxygen sa kaliwa at kanan. Sa kanan ay mayroong 2n ng carbon dioxide, dahil ang bawat molekula ay may dalawang atomo ng oxygen, kasama ang n tubig, para sa kabuuang 3n. Sa kaliwa ay may parehong bilang ng mga atomo ng oxygen na 3n, ngunit ang isa sa mga atomo ay nasa molekula ng aldehyde, na nangangahulugang dapat itong ibawas mula sa kabuuan upang makuha ang bilang ng mga atomo sa bawat molekular na oxygen. Lumalabas na ang 3n-1 atoms ay naglalaman ng molecular oxygen, na nangangahulugang mayroong 2 beses na mas kaunting mga molekula, dahil ang isang molekula ay naglalaman ng 2 atoms. Iyon ay (3n-1)/2 oxygen molecules.
Kaya, naipon namin ang isang equation para sa pagkasunog ng mga carbonyl compound sa pangkalahatang anyo.
At sa wakas ikalabindalawa ari-arian na nauugnay sa mga reaksyon ng pagpapalit halogenation sa alpha carbon atom. Muli nating buksan ang istraktura ng molekula ng aldehyde. Hinihila ng oxygen ang density ng elektron papunta sa sarili nito, na lumilikha ng bahagyang positibong singil sa carbon. Ang methyl group ay sumusubok na magbayad para sa positibong singil na ito sa pamamagitan ng pag-displace ng mga electron mula sa hydrogen patungo dito sa pamamagitan ng isang chain ng sigma bond. Ang carbon-hydrogen bond ay nagiging mas polar at ang hydrogen ay mas madaling masira kapag inaatake ng isang reagent. Ang epektong ito ay sinusunod lamang para sa alpha carbon atom, iyon ay, ang atom sa tabi ng aldehyde group, anuman ang haba ng hydrocarbon radical.
Sa ganitong paraan, posible na makakuha, halimbawa, 2-chloroacetaldehyde. Ang karagdagang pagpapalit ng mga atomo ng hydrogen sa trichloroethanal ay posible.


